|
شیمی1 نظریه سلولی: سه دانشمند به های ماتیاس اشلایدن ، تئودور شوان و رودولف فیرخو در ارائه این نظریه سهیم بودند.قبل از اینکه این نظریه را برای شما معرفی کنم سری می زنیم به کشفیات این سه دانشمند و اینکه این کشف ها چگونه به نظریه سلولی منتهی شد: رودولف فیرخو(1902-1821): ابوبکر محمّد زَکَریای رازی (۲۵۱ه.ق. – ۳۱۳ ه.ق.)پزشک، فیلسوف و شیمیدانایرانی که آثار ماندگاری در زمینهٔ پزشکی و شیمی و فلسفه نوشته است و بهعنوان کاشف الکل و جوهر گوگرد (اسید سولفوریک) مشهور است. به گفته جرج سارتن، پدر تاریخ علم، رازی «بزرگترین پزشک اسلام و قرون وسطی بود.» این دانشمند ایرانی از آنجا که کتابهای خود را به زبان عربی مینوشت، نزد غربیان به جالینوسعرب نیز مشهور بودهاست. به پاس زحمات فراوان رازی در داروسازی روز پنجم شهریورماه (۲۷ اوت)، روز بزرگداشت زکریای رازی شیمیدان بزرگ ایرانی و روز داروسازی نامگذاری شده است.
ادامه مطلب ... لویی پاستور دانشمند ، پزشک ، شیمیدان ، زیست شناس و باکتری شناس بزرگ فرانسوی در دهکده ی دل (Dole) ناحیه ی ژورا زاده شد . او در دوران کودکی هیچگونه هوش زیادی از خود نشان نمی داد ولی بسیار کوشا و بردبار بود. به خاطر اینکه از استادان خود پرسش های شگفت آوری می کرد ، از گروه شاگردان نخبه و ارزنده به شمار می رفت .
پاستور در جهان به پدر میکروبیولوژی (میکروب شناسی) مشهور است . نام او در میان اندیشمندان و نیکوکاران جهان ،همیشه به یادگار خواهد ماند .
آزمایشهای مشهور پاستور که منجر به باطل شدن نظریه خلق الساعه شدند :
آزمایش اول :
پاستور لوله ای شیشه ای برگزید و درون آن مقداری پنبه قرار داد . سپس با کمک تلمبه ای ، مقداری هوا به درون لوله کشید . سطحی از پنبه که هوا از آنجا وارد لوله می شد ، رفته رفته رو به تیرگی گذاشت تا اینکه به کلی سیاه شد .
پاستور این پنبه را در مخلوطی از اتر و الکل وارد ساخت و آنچه را که در ته محلول رسوب کرده بود زیر میکروسکوپ ساده ی خود بررسی کرد .
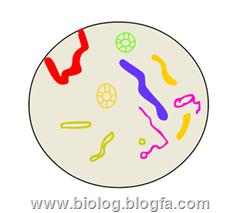
در این بررسی مشاهده کرد که ذره های گوناگون گرد و غبار ،گرده های گل ها ، باکتری ها ی فراوان ، هاگهای گوناگون و حتی تارهای پشم در رسوب وجود دارد .
پاستور از نخستین آزمایش خود نتیجه گرفت :
ادامه مطلب ... ظرفیت گرمایی ویژه(Specific heat capacity): تعریف:ظرفیت گرمایی ویژه معادل مقدار گرمایی است که لازم است مقدار مشخص از مادهای دریافت کند تا دمای آن یک واحد افزایش یابد. در سیستم استاندارد بینالمللی واحدها (SI) مقدار گرما بر حسب ژول، مقدار ماده بر حسب گرم، کیلوگرم یا مول، و تغییرات دما بر حسب سانتیگراد (که معادل تغییرات در واحد کلوین هم هست) اندازه گیری شده و یکای ظرفیت گرمایی ویژه بسته به نوع تعریف، ژول بر گرم.سانتیگراد (°J/g.C)، ژول بر کیلوگرم.سانتیگراد (°J/kg.C) یا ژول بر مول.سانتیگراد (°J/n.C) خواهد بود. درجدول زیر،ظرفیت گرمایی ویژه ی شماری ازمواد آشنارا،میبینید:
منبع:http://fa.wikipedia.org
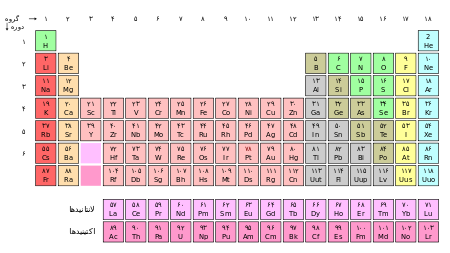
سلام دوستان.دراین مطلب ابتدا یک لینک براتون گذاشتم که باکلیک روی تصویرزیر یک جدول تناوبی تحت عنوان"جدول تناوبی پویا"میشین.خیلی جالبه،امیدوارم لذت ببرید.
جدول تناوبی عنصرهای شیمیایی، نمایش جدولی عنصرهای شیمیایی بر پایهٔ عدد اتمی، آرایش الکترونی و ویژگیهای شیمیایی آنها است. ترتیب جایگیری عنصرها در این جدول از عدد اتمی کمتر به سوی عدد اتمی (شمار پروتونهای) بالاتر است. شکل استاندارد این جدول ۱۸ × ۷ است؛ عنصرهای اصلی در بالا و دو ردیف کوچکتر از عنصرها در پایین جای دارد. میتوان این جدول را به چهار مستطیل شکست، این چهار ستون مستطیلی عبارتند از: بلوک اس در سمت چپ، بلوک پی در راست، بلوک دی در وسط و بلوک اف یا همان فلزات واسطهٔ داخلی در پایین. ردیفهای این جدول، دوره و ستونهای آن یا همان ستونهای s و d و p، گروههای جدول تناوبی نام دارند. همچنین گاهی برخی از این گروههای نامهای ویژهای دارند برای نمونه گروه هالوژنها و گازهای نجیب از آن جملهاند. هدف از ساخت جدول تناوبی چه به شکل مستطیلی و چه به شکلهای دیگر برای بررسی بهتر ویژگیهای شیمیایی عنصرها بوده است این جدول کاربرد زیادی در دانش شیمی و پردازش رفتار عنصرها دارد. اعتبار جدول تناوبی به پای دیمیتری مندلیف نوشته شده است با اینکه پیشروان دیگری پیش از او وجود داشتهاند. او این جدول را در سال ۱۸۶۹ منتشر کرد این نخستین جدولی بود که به این گستردگی مرتب شده بود. مندلیف این جدول را درست کرد تا ویژگیهای دورهای آنچه که بعدها «عنصر» نام گرفت را بهتر نشان دهد. وی توانسته بود برخی ویژگیهای عنصرهایی که هنوز کشف نشده بود را پیشبینی کند و جای آنها را خالی گذاشته بود. کم کم با پیشرفت دانش، عنصرهای تازه تری شناسایی شد و جای خالی عنصرها در جدول پُر شد. با شناسایی عنصرهای نو و گسترش شبیه سازیهای نظری دربارهٔ رفتار شیمیایی مواد، جدول آن روز مندلیف بسیار گستده تر شده است. همهٔ عنصرهای شیمیایی از عدد اتمی ۱ (هیدروژن) تا ۱۱۸ (آناناکتیوم) شناسایی یا ساخته شدهاند. دانشمندان هنوز به دنبال ساخت عنصرهای پس از آناناکتیوم اند و البته این پرسش را پیشرو دارند که عنصرهای تازه تر چگونه جدول را اصلاح خواهند کرد. همچنین ایزوتوپهای پرتوزای بسیاری هم در آزمایشگاه ساخته شده است. منبع:http://fa.wikipedia.org
مصرف آشکار و نهان آب (Overt and covert use of water)مصرف آشکارآب:مقدارآبی که روزانه به طور آشکار مصرف میشود وقابل اندازه گیری میباشد.برای مثال:آبی که برای آشامیدن درروز استفاده می کنیم. مصرف نهان آب:مقدارآبی که روزانه به طور آشکارمصرف نمیشودوقابل اندازه گیری نمیباشد.برای مثال:آبی که برای تولیدنان صرف میشود. تحقیقات آماری در بسیاری از کشورها نشان میدهد که میانگین مصرف روزانه آب برای هر نفر ، حدود 300 لیتر است. در حالی که مصرف نهان آب برای هر نفر ، حدود 6000 لیتر(20برابرمصرف آشکار)و از قرار زیر میباشد:
1.آبیاری کشتزارها و تهیه و تولید مواد غذایی برای هر نفر در روز : 2600 لیتر 2.تأمین انرژی برای هر نفر در روز : 2400 لیتر 3.صنایع و معادن برای هر نفر در روز : 700 لیتر 4.امور بازرگانی و خدمات برای هر نفر در روز : 34 لیتر پس مصرف اشکارا و نهان اب برای هر نفر در طول روز به قرار زیر است: بیش از 6300 لیتر در طول روز
سیستم استاندارد بین المللی یکاها (SI) در سال 1960 در یازدهمین کنفرانس بین المللی اوزان و اندازه ها تاسیس شد. واحد اختصاری آن در تمام جهان (SI (system international unit است. ( لازم به ذکر است این نام از زبان فرانسه آمده). این کمیت ها پایه دستگاه های بین المللی یکاها را تشکیل می دهد. حال به معرفی چندکمیت در SIمی پردازیم.
نمادگذاری علمی:برای بیان مقادیر خیلی بزرگ یا خیلی کوچک که اغلب در فیزیک با آن رو به رو می شویم از نماد گذاری علمی که توان های 10 را به کار می گیرد استفاده می کنیم. این پیشوندها را برای تمام واحد های SI می توان به کار برد. برای مثال 0.001 ثانیه را می توان یک میلی ثانیه (ms) نامید.
تفاوت وزن و جرم اغلب وقتی افراد در موضوع وزن و جرم صحبت می کنند، هر دو را از یک کمیت می دانند و با واحد کیلوگرم مشخص می کنند، در صورتی که وزن و جرم دو کمیت متفاوت هستند و تفاوت آنها در موارد زیر است:
منبع:http://qaen-amoozesh.blogfa.com
بسیاری از جوامع یا افراد قدر نعمت های موجود را نمی دانند و این قدرنشناسی را بهره برداری نادرست از این نعمت ها نشان می دهند. یکی از این نعمت های بزرگ خداوند ، آب است. چون منابع آب محدود است باید در استفاده از آنها دقت کافی به عمل آید.
آبیاری به هنگام ظهر که گرمای هوا سبب افزایش تبخیر می شود ، مقدار زیادی از آب را هدر میدهد. ادامه مطلب ...
باسلام.درابتدا براتون2انیمیشن مربوط به چرخه آب گذاشتم که باکلیک روی هرکدوم ازاعدادزیر یکیش براتون پخش میشه:
*1* *2* چرخه ی آب (Water Cycle)
گردش آب در طبیعت که به آن «چرخهی آب» یا «چرخهی هیدرولوژی» گفته میشود، عبارت است از حرکت و جابجایی آب در قسمتهای مختلف کرهی زمین.
چرخهی آب، وجود و حرکت آب را در سطح، زیر سطح و همچنین بالای کرهی زمین نشان میدهد. آب در کـرهی زمین همیشه در حال حـرکت و تغییـر شکل میباشد. زمان پیـدایش آب بر روی کـرهی زمیـن حدود 4 میلیارد سال پیش بوده و چرخهی آب میلیاردها سال است که در حال کار میباشد و زندگی همهی جانداران به آن بستگی دارد.
ادامه مطلب ...
درباره وبلاگ سلام خدمت دوستان عزیز.ممنون که به وبلاگم اومدین.امیدوارم که بارضایت ازاینجا خارج بشید.راستی بانظراتتون دلگرمم کنید. آخرین مطالب نويسندگان موضوعات پيوندها
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||







 آمار
وب سایت:
آمار
وب سایت: